Institut Charles Sadron News
Publié le 26/02/2025 par Bigo--Simon Alexis
Les hydrogels supramoléculaires sont
des matériaux dont la cohésion est généralement assurée par une
architecture nanofibreuse résultant de l’assemblage des briques
moléculaires. Lorsqu’ils sont constitués de peptides, ils font l’objet
d’un fort engouement en raison de leurs potentielles applications dans
le domaine biomédical. Ils pourraient en effet jouer le rôle de matrices
pour la libération contrôlée de médicaments ou être utilisés pour la
régénération tissulaire grâce à leurs propriétés biomimétiques.
Les
propriétés physico-chimiques de ces matériaux trouvent leur origine
dans l’organisation spatiale des peptides interagissant entre eux au
sein des nanofibres. Si de nombreuses techniques d’analyse spectrale
permettent d’apporter des informations sur cet arrangement spatial des
peptides, il n’existe aucun outil à disposition du chimiste ou du
physico-chimiste qui permette de visualiser de quelle manière ces motifs
s’assemblent à l’échelle quasi-atomique. Pourtant, cette information
est essentielle pour comprendre, concevoir et optimiser les propriétés
et performances des hydrogels supramoléculaires.
S’inspirant
de la résolution de structures iologiques obtenues par reconstruction
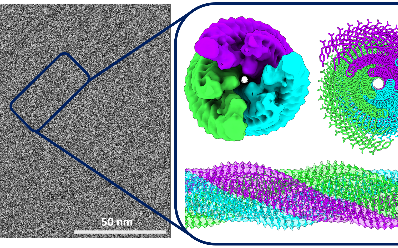
d’images haute résolution de cryo-microscopie électronique (cryo-ME)1, une approche mise à l’honneur en 2017 par l’attribution du Prix Nobel de Chimie, un consortium d’équipes de recherche2 piloté par l’Institut Charles Sadron (CNRS) pu visualiser la structure d’une nanofibre3 de
4,9 nm de diamètre avec une résolution exceptionnelle de quelques
angstrœms. Les scientifiques ont mis en évidence les groupements
moléculaires qui contribuent au cœur hydrophobe de la nanofibre et ceux
qui interagissent avec l’eau environnante de l’hydrogel. Ils révèlent
également une organisation spatiale originale des peptides interagissant
entre eux au sein des nanofibres baptisée « fermeture éclair ». Une
organisation que l’on retrouve fréquemment dans les associations de
motifs en forme d’hélice mais qui n’avait encore jamais été mise en
évidence dans ce type de nanostructures organiques supramoléculaires.
Ces
travaux sont avant tout le résultat d’une prouesse technique qui
illustre le potentiel de la reconstruction par cryo-ME pour répondre à
des questions relevant des domaines de la chimie supramoléculaire ou des
matériaux mous. Ils contribuent ainsi à une meilleure compréhension de
l’assemblage et de l’organisation dans l’espace des peptides et de leurs
acides aminés en révélant, avec une résolution rarement atteinte, des
motifs supramoléculaires inédits au sein des nanofibres.
Référence
Alexis Bigo-Simon, Leandro F.
Estrozi, Alain Chaumont, Rachel Schurhammer, Guy Schoehn, Jérôme
Combet, Marc Schmutz, Pierre Schaaf & Loïc Jierry
3D
Cryo-Electron Microscopy Reveals the Structure of a
3-Fluorenylmethyloxycarbonyl Zipper Motif Ensuring the Self-Assembly of
Tripeptide Nanofibers
ACS Nano 2024
https://doi.org/10.1021/acsnano.4c08043
- La
cryo-microscopie électronique est une technique qui permet de visualiser
des échantillons biologiques dans leur natif hydraté. Ces échantillons
sont exposés à un faisceau d électrons dans un microscope électronique,
et les images obtenues ont traitées pour reconstruire les structures
tridimensionnelles. - Ces travaux de
recherche soutenus par la Fondation Jean-Marie Lehn (Labex CSC) et l
Agence Nationale de la Recherche ont été menés en étroite collaboration
entre l’unité Biomatériaux et bioingénierie (INSERM/CNRS/Université de
Strasbourg), l Institut de biologie tructurale de Grenoble (Université
de Grenoble, CEA, CNRS), la Faculté de chimie de l Université de
Strasbourg (Chimie de la Matière Complexe) et l Institut Charles Sadron
(CNRS). - L assemblage de la
nanofibre repose sur l interaction de tripeptides amphiphiles de
séquence Phe-Phe-Tyr protégés par un groupement Fmoc en position
N-terminale, appelés Fmoc-FFY (Phe ou F, phénylalanine ; Tyr ou Y,
tyrosine ; Fmoc, fluorénylméthoxycarbonyle).